דו"ח שוק טכנולוגיות עריכת גנים מבוססות ננואינוקציה 2025: ניתוח מעמיק של דרייברי צמיחה, חידושים והשפעה גלובלית. גלו מגמות מפתח, דינמיקה תחרותית והזדמנויות אסטרטגיות שעצבו את חמש השנים הבאות.
- סיכום מנהלי וסקירת שוק
- מגמות טכנולוגיות מפתח בעריכת גנים מבוססת ננואינוקציה
- נוף תחרותי ושחקנים מובילים
- גודל השוק, תחזיות צמיחה וניתוח CAGR (2025–2030)
- ניתוח שוק אזורי ואזורי חמות מתפתחות
- אתגרים, סיכונים ושיקולים רגולטוריים
- הזדמנויות והמלצות אסטרטגיות
- תחזית עתידית: חידושים והתפתחות השוק
- מקורות והפניות
סיכום מנהלי וסקירת שוק
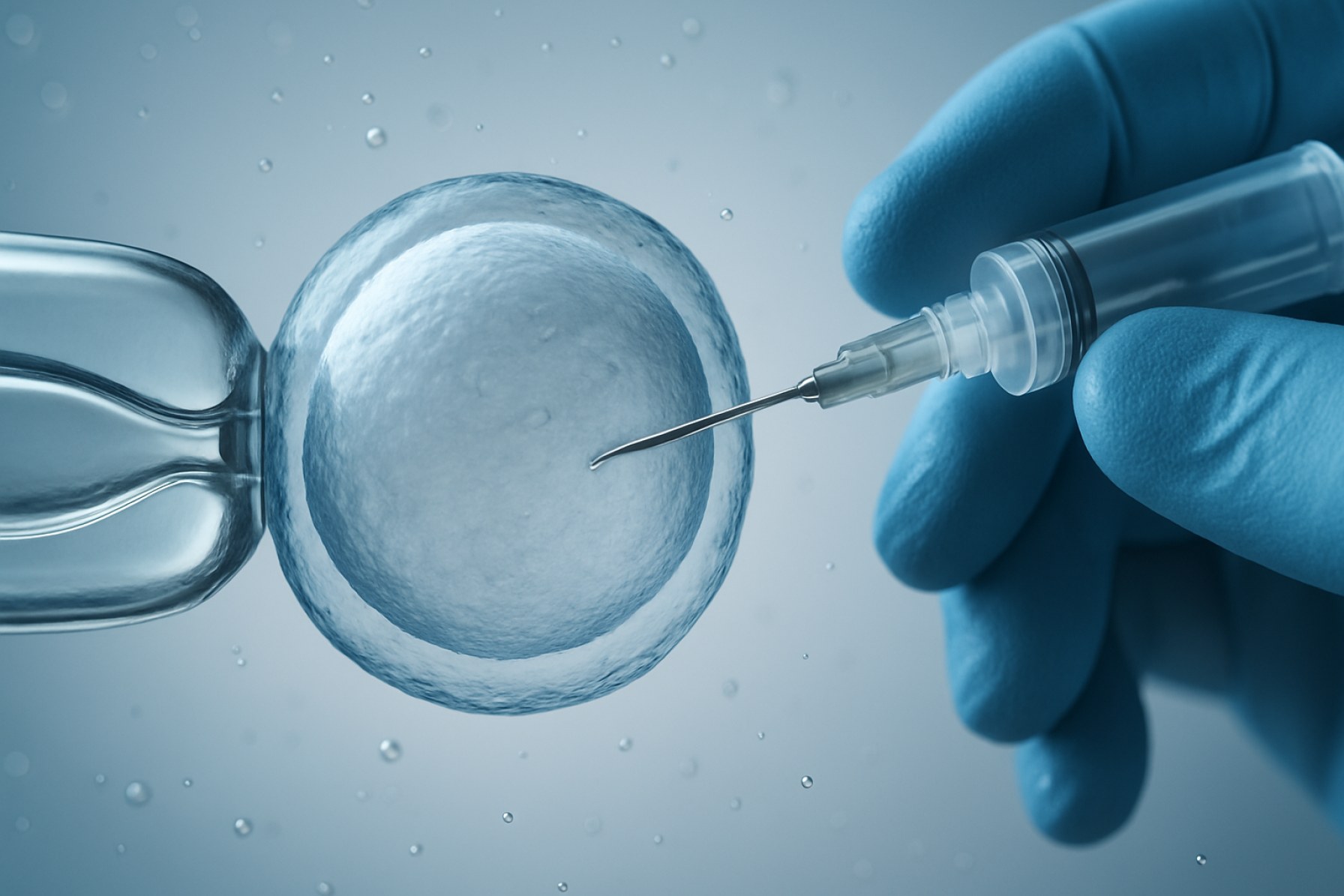
טכנולוגיות עריכת גנים מבוססות ננואינוקציה מהוות גישה מתקדמת בתחום הנדסת הגנום, מנצלות מכשירים בקנה מידה ננו כדי להעביר חומר גנטי ישירות לתוך תאים בדיוק גבוה ומינימום רעילות תאית. בניגוד לשיטות המסורתיות כמו וקטורי וירוס או אלקטרופורציה בכמות גדולה, ננואינוקציה עושה שימוש בננודקים או בננופיפטים כדי להחדיר פיזית חומצות גרעין, קומפלקסי CRISPR-Cas או כלים נוספים לעריכת גנים לתוך תאי היעד. שיטה זו מציעה יתרונות משמעותיים מבחינת יעילות השינוע, ההחזריות של התאים והיכולת למקד סוגי תאים קשים להעברה, כולל תאים ראשוניים ותאי גזע.
נכון לשנת 2025, השוק הגלובלי עבור טכנולוגיות עריכת גנים מבוססות ננואינוקציה חווה צמיחה רבה, המנוגנת על ידי ביקוש גובר לתרפיות גנים מדויקות, התקדמות בננופברקציה והחלה מתרחבת של עריכת גנים הן בהגדרות מחקריות והן קליניות. על פי Grand View Research, השוק הכולל של עריכת גנים צפוי להגיע ל-25.5 מיליארד דולר עד 2030, כשצפויות טכנולוגיות ננואינוקציה לתפוס נתח גובר בשל יכולותיהן הייחודיות. האימוץ של ננואינוקציה בולט במיוחד בתעשיית ייצור תרפיות תאים ex vivo, שם שמירה על שלמות התאים קריטית ליעילות טיפולית.
שחקני תעשייה מרכזיים, כולל חברות כמו Nanoneedle Technologies וקבוצות מחקר אקדמיות כמו אוניברסיטת סטנפורד, נמצאים בחזית המסחר של פלטפורמות אלו. שיתופי פעולה אסטרטגיים בין חברות ביוטכנולוגיה ומוסדות מחקר מאיצים את התרגום של ננואינוקציה מהמצאות מעבדתיות ליישומים קליניים. בנוסף, סוכנויות רגולטוריות כמו מינהל המזון והתרופות של ארה"ב (FDA) משתפות פעולה יותר עם המפתחים כדי להקים תקני בטיחות ויעילות עבור מוצרים מבוססי ננואינוקציה.
באופן אזורי, אמריקה הצפונית ואירופה שולטות בשוק, נתמכות בתשתיות M&D חזקות, סביבות מימון נוחות וריכוז גבוה של ניסויים קליניים בטיפול בגנים. עם זאת, אזור אסיה-פסיפיק מתפתח כאזור צמיחה משמעותי, עם מדינות כמו סין ויפן שמשקיעות רבות בננוטכנולוגיה ורפואה רגנרטיבית.
לסיכום, טכנולוגיות עריכת גנים מבוססות ננואינוקציה מצוותות לשנות את הנוף של רפואה גנטית על ידי יצירת שינויים גנטיים בטוחים, יעילים וממוקדים ביותר. תחזית השוק לשנת 2025 מאופיינת בחידוש מהיר, השקעה גוברת ואימוץ קליני מתרחב, מה שממקם את ננואינוקציה כטכנולוגיה מרכזית בדור הבא של תרפיות גנים.
מגמות טכנולוגיות מפתח בעריכת גנים מבוססת ננואינוקציה
טכנולוגיות עריכת גנים מבוססות ננואינוקציה מתפתחות במהירות, מונעות על ידי הצורך בהעברת חומר גנטי חיה, מדויקת ויעילה ומינימלית. בניגוד לשיטות המסורתיות כמו וקטורי וירוס או אלקטרופורציה בכמות גדולה, ננואינוקציה מנצלת מכשירים בקנה מידה ננו – לעיתים קרובות עשויים מסיליקון או חומרים ביocompatible אחרים – כדי להחדיר פיזית חומצות גרעין, חלבונים או רכיבי CRISPR-Cas ישירות לתוך תאי היעד. גישה זו מציעה יתרונות משמעותיים מבחינת החזריות התאית, יכולת המיקוד והיכולת למניפולציה של סוגי תאים קשים להעברה, כמו נוירונים ראשוניים או תאי גזע.
מגמות הטכנולוגיה המרכזיות שמעצב את נוף עריכת הגנים מבוססות ננואינוקציה בשנה 2025 כוללות:
- אינטגרציה עם מערכות CRISPR: ההתכנסות של פלטפורמות ננואינוקציה עם CRISPR-Cas9 וכלי עריכה גנטיים מהדור הבא מאפשרת שינויים גנטיים ממוקדים מאוד. חברות ומוסדות מחקר מפתחים מערכות ננואינוקציה המסוגלות להעביר קומפלקסי ריבונוקלאופורנוטיד (RNPs) ביעילות גבוהה, מפחיתות השפעות לא מכוונות ומגבירות את דייקנות העריכה (Nature Biotechnology).
- פלטפורמות אוטומטיות וגבוהות-עוצמה: ההתפתחויות האחרונות מתמקדות באוטומציה של תהליך הננואינוקציה, ומאפשרות עיבוד מקביל של אלפי תאים. זה רלוונטי במיוחד ליישומים בייצור תרפיות תאים וגנומיקה פונקציונלית, שבהם skalabilty וחזרות הם קריטיים (Thermo Fisher Scientific).
- חידושי חומרים: הפיתוח של חומרים חדשים לננואינוקציה – כמו פולימרים גמישים, צינורות פחמן וחומרים קומפוזיטיים היברידיים – משפר את הביocompatibility ומפחית את הלחץ התאי. חידושים אלו מרחיבים את מגוון סוגי התאים המתאימים לננואינוקציה וממזערים את הרעילות התאית (Nano Today).
- מעקב בזמן אמת ותגובות: אינטגרציה של ננסנזורים ומודלים דימויים עם מכשירי ננואינוקציה מאפשרת מעקב בזמן אמת של אירועי השינוע ותגובות תאים. לולאת משוב זו משפרת את שליטת התהליך ותומכת בפיתוח פרוטוקולים אדפטיביים לעריכת גנים (Trends in Biotechnology).
מגמות אלו יחדיו דוחפות את האימוץ של טכנולוגיות עריכת גנים מבוססות ננואינוקציה בהגדרות מחקריות וקליניות כאחד, עם מספר הולך וגדל של סטארטאפים ושחקנים מבוססים המשקיעים בפלטפורמות העברת דור הבא. ככל שהטכנולוגיה מתבגרת, צפויה לשחק תפקיד קרדינלי בהתקדמות של רפואה מותאמת, תרפיות רגנרטיביות ומחקר גנומיקה פונקציונלית.
נוף תחרותי ושחקנים מובילים
הנוף התחרותי עבור טכנולוגיות עריכת גנים מבוססות ננואינוקציה בשנת 2025 מאופיין בתערובת דינמית של חברות ביוטכנולוגיה מבוססות, סטארטאפים חדשניים ומקבילויות אקדמיות, כולן מתמודדות על מנהיגות בשינוע מדויק של גנים. ננואינוקציה, אשר מנצלת מכשירים בקנה מידה ננו כדי להעביר פיזית חומר גנטי לתוך תאים, הולכת ותופסת תאוצה כאלטרנטיבה מבטיחה לשיטות מסורתיות של העברה כימית ווויראלית בזכות יעילותה הגבוהה ורעילותה המופחתת.
שחקנים מרכזיים במרחב זה כוללים את Thermo Fisher Scientific, שהרחיבה את פורטפוליו עריכת הגנים שלה דרך רכישות ושיתופי פעולה אסטרטגיים, ו-Lonza Group, הידועה בפלטפורמות המתקדמות שלה לייצור תרפיות תאים וגנים. שתי החברות משקיעות במחקר ופיתוח של ננואינוקציה על מנת לשפר את דיוק השינוע ואת Scalability של היישומים הקליניים.
חברות מתפתחות כמו NanoCellect Biomedical ו-Nanolive מבצעות צעדים משמעותיים על ידי פיתוח מכשירי ננואינוקציה פרופאייתריים המיועדים לעריכת גנים בהיקף גבוה בהגדרות מחקריות ותרפויטיות. חברות אלו מתמקדות במערכות מיני אוטומטיות המאפשרות שינוע מהיר וחוזר של CRISPR-Cas9 וכלי עריכת גנים אחרים בתוך מגוון רחב של סוגי תאים, כולל תאים ראשוניים קשים להעברה.
מקבילויות אקדמיות, כמו אלו שמקורן בשיתופי פעולה עם מוסדות כמו אוניברסיטת סטנפורד ו-MIT, תורמות גם הן לנוף התחרותי על ידי מסחר של פלטפורמות ננואינוקציה חדשות. ישויות אלו נהנות לעיתים קרובות ממימון בשלבים מוקדמים ושיתופי פעולה עם חברות ביוטכנולוגיה גדולות כדי להאיץ את פיתוח המוצרים ואת האישור הרגולטורי.
השוק מעוצב עוד יותר על ידי פעילות פטנטים מתמשכת והסכמי רישוי, כאשר חברות שואפות להגן על טכנולוגיות ננואינוקציה הייחודיות שלהן ולהרחיב את היקף השימוש שלהן. לפי דו"ח משנת 2024 מאת Grand View Research, צפוים שוק עריכת הגנים הגלובלי לגדול בסך של יותר מ-15% עד 2030, כאשר הגישות מבוססות ננואינוקציה תופסות נתח גובר בזכות הפוטנציאל שלהן לתרפיות גנים בטוחות וממוקדות יותר.
- Thermo Fisher Scientific ו-Lonza Group מובילים באינטגרציית פלטפורמות ובתרגום קליני.
- NanoCellect Biomedical ו-Nanolive מקדמים חידושים במיניאטיזציה של מכשירים ואוטומציה.
- מקבילויות אקדמיות מאיצות את העברת טכנולוגיה משבשת ואימוץ מוקדם.
באופן כללי, הנוף התחרותי בשנת 2025 מאופיין בחידוש מהיר, שיתופי פעולה אסטרטגיים ומיקוד בפתרונות ננואינוקציה ברמת קלינית, מה שממקם את המגזר לצמיחה והשפעה משמעותית בטיפולי גנים ורפואה רגנרטיבית.
גודל השוק, תחזיות צמיחה וניתוח CAGR (2025–2030)
השוק הגלובלי עבור טכנולוגיות עריכת גנים מבוססות ננואינוקציה צפוי להתרחב בצורה מרשימה בין השנים 2025 ל-2030, מונע על ידי אימוץ מואץ גם בשימושים מחקריים וגם תרפויטיים. ננואינוקציה, שמאפשרת העברה מדויקת של חומר גנטי לתוך תאים עם מינימום רעילות, הולכת ותופסת העדפה על פני שיטות העברה מסורתיות כמו העברה כימית ומיקרואינוקציה, בעיקר בהקשר של CRISPR וכלי עריכת גנים אחרים.
על פי תחזיות של Grand View Research, השוק הכולל של עריכת גנים צפוי להגיע ליותר מ-25 מיליארד דולר עד 2030, כאשר הגישות מבוססות ננואינוקציה ממלאות תפקיד הולך וגדל בזכות יעילותן המוגברת והScalability שלהן. בעוד מספרים ספציפיים עבור ננואינוקציה פחות מושגים לעיתים קרובות, ניתוחים תעשייתיים מציעים כי המגזר הזה יחווה שיעור צמיחה שנתי מצטבר (CAGR) של approximately 18–22% משנת 2025 עד 2030, ויעלה את שיעור צמיחה המצטבר של השוק הכולל של עריכת גנים שקורא שיעור צמיחה של 15–17% באותו פרק זמן.
דרייברים עיקריים של צמיחה זו כוללים:
- ביקוש גובר לעריכת גנים מדויקת בשרשרת טיפול תאים וגנים, במיוחד עבור שינוי ex vivo של תאי גזע ותאי חיסון.
- השקעה מרובות בננוטכנולוגיה עם מערכות העברה על ידי חברות ביוטכנולוגיה מובילות כמו Thermo Fisher Scientific ו-Lonza Group, שהן פעילה מפתחות פלטפורמות ננואינוקציה פרופייטריות.
- הרחבת היישומים בביוטכנולוגיה חקלאית, בה ננואינוקציה משמשת ליצירת צמחים מהונדסים גנטית עם תכונות משופרות.
באופן אזורי, צפויה אמריקה הצפונית לשמור על נתח השוק הגדול ביותר עד 2030, נתמכת על ידי תשתית M&D חזקה ודרכים רגולטוריות נוחות. עם זאת, אזור אסיה-פסיפיק צפוי להציג את ה-CAGR המהיר ביותר, מונע על ידי מימון ממשלתי גובר וצמיחת שחקנים מקומיים שמחפשים להשקיע בטכנולוגיות עריכת גנים מתקדמות (MarketsandMarkets).
לסיכום, שוק טכנולוגיות עריכת גנים מבוססות ננואינוקציה מגיע לצמיחה משמעותית מ-2025 עד 2030 עם שיעור צמיחה משוער של 18–22%. התפתחות זו תשתפר על ידי חידושים טכנולוגיים, הרחבת ההיקף ליישומים ושקעות אסטרטגיות משני משתתפי תעשייה מבוססים ומתפתחים.
ניתוח שוק אזורי ואזורי חמות מתפתחות
נוף השוק האזורי עבור טכנולוגיות עריכת גנים מבוססות ננואינוקציה בשנת 2025 מאופיין בהבדלים חשובים באימוץ, השקעה ומסגרות רגולטוריות. אמריקה הצפונית, ובמיוחד ארצות הברית, ממשיכה להיות השוק השולט, מונע על ידי מימון יציב ב-M&D, ריכוז גבוה של חברות ביוטכנולוגיה ודרכים רגולטוריות תומכות. נוכחותם של מוסדות אקדמיים מובילים ושיתופי פעולה בין תעשייה לארגוני מחקר האיצו את המסחר של פלטפורמות ננואינוקציה לשימושים תרפויטיים וחקלאיים. על פי Grand View Research, אמריקה הצפונית אחזקה ב-40% מהשוק הגלובלי של עריכת גנים בשנת 2024, כאשר טכנולוגיות ננואינוקציה צוברות תאוצה הודות לדיוקן ועל יעד השפעות מצומצמות.
אירופה עוקבת מקרוב, כאשר מדינות כמו גרמניה, בריטניה וצרפת משקיעות רבות בכלים החדשים לעריכת גנים מהדור הבא. תוכנית האופק של האיחוד האירופי, Horizon Europe, הקצתה מימון משמעותי לננוטכנולוגיה ולהנדסת גנום, תוך יצירת סביבה תחרותית לסטארטאפים ולשחקנים מבוססים כאחד. עם זאת, הסביבה הרגולטורית המחמירה של האזור, במיוחד בכל הנוגע לאורגניזמים מהונדסים גנטית (GMOs), מציבה אתגרים להפצת השוק המהירה. עם זאת, הגישה המתפתחת של סוכנות התרופות האירופאית לגבי תרפיות מתקדמות צפויה להקל על אימוץ קליני גדול יותר של גישות מבוססות ננואינוקציה בשנים הקרובות (European Medicines Agency).
אזור אסיה-פסיפיק מתפתח כאזור חם, עם סין, יפן ודרום קוריאה העושות השקעות אסטרטגיות במחקר ננואינוקציה ותשתיות. יוזמות מגובות ממשלת סין והתרחבות מואצת של סטארטאפים ביוטכנולוגיים מימשו את המדינה כמחדש מפתח בתחום. הסביבה הרגולטורית היחסית הגמישה של האזור ואוכלוסיות המטופלים הגדולות מושכות שיתופי פעולה בין-לאומיים וניסויים קליניים. על פי Fortune Business Insights, אזור אסיה-פסיפיק צפוי להציג את ה-CAGR המהיר ביותר במגזר עריכת הגנים עד 2027, כאשר טכנולוגיות ננואינוקציה משחקות תפקיד מרכזי בתחום הביולוגיה החקלאית ורפואה רגנרטיבית.
- אמריקה הצפונית: מנהיגות שוק, M&D חזקה, מגמות רגולטוריות נוחות.
- אירופה: השקעה גבוהה, מכשולים רגולטוריים, אימוץ קליני הולך וגדל.
- אסיה-פסיפיק: הצמיחה המהירה ביותר, תמיכה ממשלתית, הרחבת יישומים קליניים וחקלאיים.
אזורי חמות נוספים כוללים את ישראל וסינגפור, שם תמריצים ממשלתיים ומיקוד במחקר תרגומי מעודדים חידושים בטכנולוגיות עריכת גנים מבוססות ננואינוקציה. אזורים אלו צפויים לתרום לנוף התחרותי הגלובלי, במיוחד בתחומים תרפויטיים נישתיים ובמדעי היבול.
אתגרים, סיכונים ושיקולים רגולטוריים
טכנולוגיות עריכת גנים מבוססות ננואינוקציה, אשר משתמשות במכשירים בקנה מידה ננו כדי להעביר חומר גנטי ישירות לתאים, מציגות אלטרנטיבה מבטיחה לשיטות העברה ויראליות וכימיות מסורתיות. עם זאת, כאשר טכנולוגיות אלו מתקדמות לעבר אימוץ רחב קליני ומסחרי בשנת 2025, ישנם מספר אתגרים, סיכונים ושיקולים רגולטוריים שיש להתייחס אליהם.
אחד האתגרים הטכניים העיקריים הוא השגת יעילות העברה ושרידות תאים אחידות בכל סוגי התאים. בעוד שננואינוקציה יכולה להפחית רעילות בהשוואה לחלק משיטות כימיות, החדירה המכנית של ממברנות התאים עדיין מהווה סיכון לנזק לתא ולתגובות חיסוניות לא מכוונות. בנוסף, היכולת להרחיב פלטפורמות ננואינוקציה ליישומים בהיקף גבוה נשארת מכשול משמעותי, כשמערכות נוכחיות דורשות לעיתים קרובות יישור ושליטה מדויקים שקשה לאוטומט על גבי סקלאות תעשייתיות (Nature Biotechnology).
מפרספקטיבת סיכון, השפעות לא מכוונות ויציבות גנומית הם חששות קריטיים. אף על פי שננואינוקציה מאפשרת העברה מדויקת, כלי עריכת הגנים עצמם (כגון CRISPR-Cas9) עדיין יכולים להכניס מוטציות בלתי מכוונות. ההשפעות ארוכות הטווח של עריכות אלו, במיוחד בהקשרים תרפויטיים, עדיין אינן מובנות לחלוטין. יתרה מכך, השימוש בננומרים מציג פוטנציאל רעילות ועדכנות ביוכימית, מכיוון שהגורל של ננופרטיקלים בתוך הגוף ואינטראקציות שלהם עם מערכות ביולוגיות דורשים חקירה מעמיקה (U.S. Food and Drug Administration).
- אי ודאות רגולטורית: המסגרות הרגולטוריות עבור טכנולוגיות עריכת גנים מבוססות ננואינוקציה עדיין מתפתחות. סוכנויות כמו ה-FDA והסוכנות התרופות האירופאית מפתחות מדריכים עבור הן ננוטכנולוגיה והן עריכת גנים, אך תקנים מגובשים חסרים. זה יוצר אי ודאות למפתחים לגבי דרישות ניסויים קליניים, הערכות בטיחות ומעקב לאחר השוק.
- שיקולים אתיים וחברתיים: הפוטנציאל לעריכת גנים של קווי תקשורת ושינויים גנטיים גנטיים מעלה שאלות אתיות, במיוחד במדינות שבהן ישנם רגולציות מחמירות על השינוי הגנטי האנושי. התפיסה הציבורית וההסכמה של תרפיות מבוססות ננואינוקציה עשויות גם להשפיע על החלטות רגולטוריות ואימוץ שוק (Nature).
לסיכום, בעוד שטכנולוגיות עריכת גנים מבוססות ננואינוקציה מציעות יתרונות משמעותיים, הדרך שלהן לשימוש נרחב בשנת 2025 מעוצבת על ידי אתגרים טכניים, בטיחותיים ורגולטוריים שדורשים מאמצים מתואמים מתעשייה, רגולטורים והקהילה המדעית.
הזדמנויות והמלצות אסטרטגיות
שוק טכנולוגיות עריכת גנים מבוססות ננואינוקציה בשנת 2025 מציע נוף דינמי של הזדמנויות, שנובע מהתכנסות רפואה מדויקת, ננוטכנולוגיה מתקדמת והביקוש הגובר לזרועות העברת גנים יעילות. ננואינוקציה, המנצלות מחטי ננו או חיישנים כדי להעביר חומר גנטי ישירות לתוך תאים, מציעות יתרונות משמעותיים על פני שיטות העברה מסורתיות כמו העברה כימית וויראלית, תוך הפחתת רעילות, שיפור יעילות זרימת העברת הגנים והיכולת למקד סוגי תאים קשים להעברה.
ההזדמנויות המרכזיות במגזר זה נובעות מהאימוץ הגובר של תרפיות גנים עבור מחלות נדירות והתורשתיות, כמו גם מהרחבת הפייפליין של מועמדים לטיפולי תאים וגנום בניסויים קליניים. ה-FDA וה-EMA האיצו את האיומים לתרפיות גנטים, מה שמייצר סביבה רגולטורית נוחה לטכנולוגיות העברה חדשניות כמו ננואינוקציה. יתרה מכך, ההשקעה הגוברת ברפואה מותאמת ותרפיות רגנרטיביות צפויה להניע את הביקוש לכלי עריכת גנים מדויקים ומינימליים.
- שיתופי פעולה אסטרטגיים: חברות צריכות להשקיע בשיתופי פעולה עם מרכזי מחקר אקדמיים מובילים וחברות ביוטכנולוגיה כדי להאיץ את הפיתוח והאישור של פלטפורמות ננואינוקציה. שיתופי פעולה מסוג זה יכולים להקל על הגישה לכלי עריכת גנים חדשניים (למשל CRISPR, TALENs) ולהרחיב את היקף היישומים התרפויטיים. לדוגמה, בריתות עם ארגונים כמו Broad Institute או CRISPR Therapeutics יכולות להנגיש למומחיות מתקדמת בתחום עריכת הגנים.
- גיוון פלטפורמות: הרחבת יישום הננואינוקציה מעבר לרפואה אנושית על ידי הכללת ביוטכנולוגיה חקלאית, בריאות בעלי חיים וביולוגיה סינתטית יכולים לפתוח נתיבי הכנסה חדשים. במיוחד, הסקטור החקלאי מחפש פתרונות מדויקים לעריכת גנים לשיפור היבולים והתנגדות למחלות, כפי שהדגישו Syngenta ובייר.
- מעורבות רגולטורית: מעורבות פרואקטיבית עם סוכנויות רגולטוריות חיונית להקל על דרכי האישור ולהקים תקנים בתעשייה עבור מכשירי ננואינוקציה. דיאלוג מוקדם עם ה-FDA וEMA יכול לעזור לפתור חששות בטיחות ויעילות, ולהאיץ את הכניסה לשוק.
- אסטרטגיית קניין רוחני (IP): אבטחת הגנה חזקה על מכשירי ננואינוקציה ופרוטוקולים עריכת גנים קשורה קריטית לשמירה על יתרון תחרותי. חברות צריכות לעקוב אחרי נופי הפטנטים ולרדוף אחר הגשת פטנטים אסטרטגיים, כפי שמעידים על כך פעילות אחרונה מThermo Fisher Scientific ו-Lonza.
לסיכום, שוק טכנולוגיות עריכת גנים מבוססות ננואינוקציה בשנת 2025 מתייצב לצמיחה, כאשר הזדמנויות אסטרטגיות מתמקדות על שיתופי פעולה, הרחבת פלטפורמה, התאמת רגולציה וניהול קניין רוחני. חברות שמנצלות את התחומים הללו צפויות להשיג מיקום מוביל בשדה המתפתח במהירות הזה.
תחזית עתידית: חידושים והתפתחות השוק
תחזית עתידית לטכנולוגיות עריכת גנים מבוססות ננואינוקציה בשנת 2025 מאופיינת בחידוש מהיר ובתהליך התפתחות שוק דינמי, המונע על ידי התכנסות של ננוטכנולוגיה, ביולוגיה סינתטית ורפואה מדויקת. ננואינוקציה, המנצלות מכשירים בקנה מידה ננו כדי להעביר חומר גנטי ישירות לתוך תאים בדיוק גבוה, צפויה להתמודד עם מגבלות חשובות של שיטות העברת עריכת גנים מסורתיות, כמו וקטורים ויראליים ואלקטרופורציה בכמות גדולה. טכנולוגיה זו צפויה לאפשר עריכה גנטית בטוחה יותר, יעילה יותר ופחות אימונוגנית, במיוחד עבור יישומים תרפויטיים ex vivo ו-in vivo.
בשנת 2025, מספר מגמות מעצבות את נוף החידושים. ראשית, אינטגרציה של חומרים מתקדמים כגון צינורות פחמן, סרטים ננוזים ופולימרים ניתנים להידחות לתוך מכשירי הננואינוקציה משפרת את הביocompatibility ויכולת הדיוק המכוונת. חברות ומוסדות מחקר מפתחים ננואינוקטורים מהדור הבא המסוגלים להעברת מרובים, מאפשרים עריכה סימולטנית של מספר גנים או סוגי תאים, דבר קריטי למחלות מורכבות כמו סרטן ומחלות גנטיות (Nature Biotechnology).
שנית, אוטומציה ומיניאטיזציה מאיצות את Scalability של פלטפורמות ננואינוקציה. סטארטאפים ושחקנים מבוססים מציגים מערכות ננואינוקציה מבוססות מיקרופלואידים שיכולות לעבד אלפי תאים בשנייה, מה שהופך את הטכנולוגיה לנוחה יותר עבור יישומים קליניים ותעשייתיים בהיקף רחב (Thermo Fisher Scientific). זה צפוי להפחית עלויות ולשפר את החזרויות, תוך התמודדות עם מכשולים מרכזיים למסחור.
מפרספקטיבת השוק, השוק הגלובלי עבור עריכת הםל גנים צפוי להכות $15 מיליארד עד 2025, כאשר טכנולוגיות ננואינוקציה תופסות נתח הולך וגדל בזכות יתרונותיהן הייחודיות מבחינת דיוק ובטיחות (Grand View Research). שיתופי פעולה אסטרטגיים בין חברות ביוטכנולוגיה, מוסדות אקדמיים ויצרני מכשירים מאיצים את אקוסיסטם היצירה. סוכנויות רגולטוריות מתאימות גם הן את מסגרותיהן כדי להתאים לפרופילים החדשים ולפוטנציאל התרפויטי של גישות מבוססות ננואינוקציה (U.S. Food and Drug Administration).
- יישומים מתפתחים כוללים תרפיות תאים וגנום, רפואה רגנרטיבית ומחקר גנומיקה פונקציונלית.
- אתגרים מרכזיים עדיין קיימים בסטנדרטיזציה של פרוטוקולים, הבטחת בטיחות ארוכת טווח וניווט בלאנדי קניין רוחני מורכבות.
- ניסויים קליניים ממשיכים ומחקרים פרה-קליניים בשנת 2025 צפויים לספק נתונים קריטיים על יעילות ובטיחות, אשר ישפיעו על שיעורי האימוץ העתידיים.
באופן כללי, טכנולוגיות עריכת גנים מבוססות ננואינוקציה צפויות לשחק תפקיד טרנספורמטיבי בגל הסמכות הבא של רפואה גנומית, כאשר 2025 מציינת שנה חשובה הן עבור חידושים טכנולוגיים והן עבור התפשטות השוק.
מקורות והפניות
- Grand View Research
- אוניברסיטת סטנפורד
- Nature Biotechnology
- Thermo Fisher Scientific
- Nanolive
- MIT
- MarketsandMarkets
- סוכנות התרופות האירופאית
- Fortune Business Insights
- Broad Institute
- Syngenta